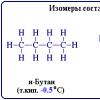
Альдегиды и кетоны – это производные углеводородов, в молекулах которых имеется карбонильная группа. Альдегиды по строению отличаются от кетонов положением карбонильной группы. О физических свойствах альдегидов и кетонов, а также об их классификации и номенклатуре говорим в этой статье.
Физические свойства
В отличие от спиртов и фенолов, для альдегидов и кетонов не характерно образование водородных связей, именно поэтому их температуры кипения и плавления значительно ниже. Так, формальдегид – газ, уксусный альдегид кипит при температуре 20,8 градусов, тогда как метанол кипит при температуре 64,7 градусов. Аналогично фенол – кристаллическое вещество, а бензальдегид – жидкость.
Формальдегид – бесцветный газ с резким запахом. Остальные члены ряда альдегидов – жидкости, а высшие альдегиды являются твердыми веществами. Низшие члены ряда (формальдегид, ацетальдегид) – растворимы в воде, имеют резкий запах. Высшие альдегиды хорошо растворимы в большинстве органических растворителях (спирты, эфиры), у альдегидов С 3 -С 8 весьма неприятный запах, а высшие альдегиды применяются в парфюмерии из-за цветочных запахов.

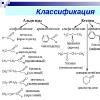
Рис. 1. Таблица классификация альдегидов и кетонов.
Общая формула альдегидов и кетонов выглядит следующим образом:
- формула альдегидов – R-COH
- формула кетонов – R-CO-R
Классификация и номенклатура
Альдегиды и кетоны отличаются по типу углеродной цепи, в которой находится карбонильная группа. Рассмотрим соединения жирного ряда и ароматические:
- ациклические, предельные . Первым членом гомологического ряда альдегидов является муравьиный альдегид (формальдегид, метаналь) – CH 2 =O.
Муравьиный альдегид применяется как антисептик. С его помощью осуществляется дезинфекция помещений, протравливание семян.
Второй член альдегидного ряда – уксусный альдегид (ацетальдегид, этаналь). Он применяется как промежуточный продукт при синтезе уксусной кислоты и этилового спирта из ацетилена.

Рис. 2. Формула уксусный альдегид.
- непредельные . Необходимо упомянуть такой непредельный альдегид, как акролеин (пропеналь). Этот альдегид образуется при термическом разложении глицерина и жиров, составной частью которых является глицерин.
- ароматические . Первым членом гомологического ряда ароматических альдегидов является бензольный альдегид (бензальдегид). Также можно отметить такой альдегид растительного происхождения, как ванилин (3-метокси-4-гидроксибензальдегид).

Рис. 3. Формула ванилин.
Кетоны могут быть чисто ароматические и жиро-ароматические. Чисто ароматическим является, например, дифенилкетон (бензофенон). Жирно-ароматическим является, например, метил-фенилкетон (ацетофенон)
Что мы узнали?
На уроках химии 10 класса важнейшей задачей является изучение альдегидов и кетонов. В альдегидах атом углерода карбонильной группы является первичным, а в кетонах вторичным. Поэтому в альдегидах карбонильная группа всегда связана с атомом водорода. Альдегидная группа обладает большей химической активностью, чем кетонная, особенно в реакциях окисления.
Тест по теме
Оценка доклада
Средняя оценка: 4.2 . Всего получено оценок: 166.
5.1. Общая характеристика
Родственные классы альдегидов и кетонов содержат функциональную карбонильную группу и относятся к карбонильным соединениям. Для них также используется общее название оксосоединения, так как группа =О называется оксогруппой.
Альдегидами называют соединения, в которых карбонильная группа связана с органическим радикалом и атомом водорода; кетонами - карбонильные соединения с двумя органическими радикалами.
Группу -СН=О, входящую в состав альдегидов, называют альдегидной, соответственно группу в кетонах - кетонной, или кетогруппой.
В зависимости от природы органических радикалов альдегиды и кетоны могут принадлежать к алифатическому или ароматическому ряду; кетоны бывают смешанными (табл. 5.1).

В отличие от спиртов в молекулах альдегидов и кетонов отсутствуют связанные с атомами кислорода подвижные атомы водорода. В связи с этим альдегиды и кетоны не ассоциированы за счет образования водородных связей, но склонны к образованию водородных связей с молекулами воды и поэтому хорошо в ней растворяются (особенно первые члены гомологического ряда).
Таблица 5.1. Альдегиды и кетоны

5.2. Реакционные центры альдегидов и кетонов
sp 2 -Гибридизованный атом углерода карбонильной группы образует три σ-связи, лежащие в одной плоскости, и π-связь с атомом кислорода за счет негибридизованной p-орбитали. Вследствие различия в электроотрицательности атомов углерода и кислорода π-связь между ними сильно поляризована (рис. 5.1). В результате на атоме углерода карбонильной группы возникает частичный положительный заряд δ+, а на атоме кислорода - частичный отрицательный заряд δ-. Поскольку атом углерода электронодефицитен, он представляет собой центр для нуклеофильной атаки.
Распределение электронной плотности в молекулах альдегидов и кетонов с учетом передачи электронного влияния электроно-

Рис. 5.1. Электронное строение карбонильной группы
дефицитного атома углерода карбонильной группы по σ-связям представлено на схеме 5.1.
Схема 5.1. Реакционные центры в молекуле альдегидов и кетонов

В молекулах альдегидов и кетонов присутствует несколько реакционных центров:
Электрофильный центр - атом углерода карбонильной группы - предопределяет возможность нуклеофильной атаки;
Основный центр - атом кислорода - обусловливает возможность атаки протоном;
СН-кислотный центр, атом водорода которого обладает слабой протонной подвижностью и может, в частности, подвергаться атаке сильным основанием.
В целом альдегиды и кетоны обладают высокой реакционной способностью.
5.3. Нуклеофильное присоединение
Для альдегидов и кетонов наиболее характерны реакции нуклеофильного присоединения A N .
Общее описание механизма нуклеофильного присоединения A N
Легкость нуклеофильной атаки по атому углерода карбонильной группы альдегида или кетона зависит от величины частичного
положительного заряда на атоме углерода, его пространственной доступности и кислотно-основных свойств среды.

С учетом электронных эффектов групп, связанных с карбонильным атомом углерода, величина частичного положительного заряда δ+ на нем в альдегидах и кетонах убывает в следующем ряду:

Пространственная доступность карбонильного атома углерода уменьшается при замене водорода более объемистыми органиче- скими радикалами, поэтому альдегиды более реакционноспособны, чем кетоны.

Общая схема реакций нуклеофильного присоединения A N к карбонильной группе включает нуклеофильную атаку по карбонильному атому углерода, за которой следует присоединение электрофила к атому кислорода.

В кислой среде активность карбонильной группы, как правило, увеличивается, поскольку вследствие протонирования атома кислорода на атоме углерода возникает положительный заряд. Кислотный катализ используют обычно тогда, когда атакующий нуклеофил обладает низкой активностью.
По приведенному выше механизму осуществляется ряд важных реакций альдегидов и кетонов.
Многие свойственные альдегидам и кетонам реакции протекают в условиях организма, эти реакции представлены в последующих разделах учебника. В настоящей главе будут рассмотрены наиболее важные реакции альдегидов и кетонов, которые в обзорном виде приведены на схеме 5.2.

Присоединение спиртов. Спирты при взаимодействии с альдегидами легко образуют полуацетали. Полуацетали обычно не выделяют из-за их неустойчивости. При избытке спирта в кислой среде полуацетали превращаются в ацетали.

Применение кислотного катализатора при превращении полуацеталя в ацеталь становится понятным из приведенного ниже механизма реакции. Центральное место в нем занимает образование карбо- катиона (I), стабилизированного за счет участия неподеленной пары электронов соседнего атома кислорода (+M-эффект группы С 2 Н 5 О).

Реакции образования полуацеталей и ацеталей обратимы, поэтому ацетали и полуацетали легко гидролизуются избытком воды в кислой среде. В щелочной среде полуацетали устойчивы, так как алкоксидион является более трудно уходящей группой, чем гидроксид-ион.
Образование ацеталей часто используется как временная защита альдегидной группы.
Присоединение воды. Присоединение воды к карбонильной группе - гидратация - обратимая реакция. Степень гидратации альдегида или кетона в водном растворе зависит от строения субстрата.
Продукт гидратации, как правило, в свободном виде выделить с помощью перегонки не удается, так как он разлагается на исходные компоненты. Формальдегид в водном растворе гидратирован более чем на 99,9%, ацетальдегид - приблизительно наполовину, ацетон практически не гидратирован.

Формальдегид (муравьиный альдегид) обладает способностью свертывать белки. Его 40% водный раствор, называемый формалином, применяется в медицине как дезинфицирующее средство и консервант анатомических препаратов.
Трихлороуксусный альдегид (хлораль) гидратирован полностью. Электроноакцепторная трихлорометильная группа настолько стабилизирует хлоральгидрат, что это кристаллическое вещество отщепляет воду только при перегонке в присутствии дегидратирующих веществ - серной кислоты и др.

В основе фармакологического эффекта хлоральгидрата СС1 з СН(ОН )2 лежит специфическое действие на организм альдегидной группы, обусловливающее дезинфицирующие свойства. Атомы галогена усиливают ее действие, а гидратация карбонильной группы снижает токсичность вещества в целом.
Присоединение аминов и их производных. Амины и другие азотсодержащие соединения общей формулы NH 2 X (X = R, NHR) реагируют с альдегидами и кетонами в две стадии. Сначала образуются продукты нуклеофильного присоединения, которые затем вследствие неустойчивости отщепляют воду. В связи с этим данный процесс в целом классифицируют как реакцию присоединения-отщепления.

В случае первичных аминов получаются замещенные имины (их называют также основаниями Шиффа).
Имины - промежуточные продукты многих ферментативных процессов. Получение иминов проходит через стадию образования аминоспиртов, которые бывают относительно устойчивы, например при взаимодействии формальдегида с α-аминокислотами (см. 12.1.4).
Имины являются промежуточными продуктами получения аминов из альдегидов и кетонов путем восстановительного аминирования. Этот общий способ заключается в восстановлении смеси карбонильного соединения с аммиаком (или амином). Процесс протекает по схеме присоединения-отщепления с образованием имина, который затем восстанавливается в амин.
При взаимодействии альдегидов и кетонов с производными гидразина получаются гидразоны. Эту реакцию можно использовать для выделения альдегидов и кетонов из смесей и их хроматографической идентификации.

Основания Шиффа и другие подобные соединения легко гидролизуются водными растворами минеральных кислот с образованием исходных продуктов.
В большинстве случаев для реакций альдегидов и кетонов с азотистыми основаниями необходим кислотный катализ, ускоряющий дегидратацию продукта присоединения. Однако если слишком повысить кислотность среды, то реакция замедлится в результате превращения азотистого основания в нереакционноспособную сопряженную кислоту XNH 3+.
Реакции полимеризации. Эти реакции свойственны в основном альдегидам. При нагревании с минеральными кислотами полимеры альдегидов распадаются на исходные продукты.
Образование полимеров можно рассматривать как результат нуклеофильной атаки атомом кислорода одной молекулы альдегида карбонильного атома углерода другой молекулы. Так, при стоянии формалина выпадает в виде белого осадка полимер формальдегида - параформ.
5.4. Реакции конденсации
Наличие СН-кислотного центра в молекуле альдегида или кетона приводит к тому, что α-атомы водорода этих карбонильных соединений обладают некоторой протонной подвижностью. Под действием оснований такие протоны могут отщепляться с образованием соот- ветствующих карбанионов. Карбанионы играют роль нуклеофилов по отношению к карбонильному субстрату. Это обусловливает возможность осуществления реакций, в которых одна молекула в качестве нуклеофила присоединяется к карбонильной группе другой молекулы нейтрального карбонильного соединения. Такие процессы относятся к реакциям конденсации.
Конденсацией называют реакцию, приводящую к возникновению новой углерод-углеродной связи, причем из двух или нескольких относительно простых молекул образуется новая, более сложная молекула.
Так, в щелочной среде из двух молекул ацетальдегида образуется гидроксиальдегид с удвоенным числом атомов углерода.
Продукт реакции, содержащий гидроксильную и альдегидную группы, называется альдолем (от слов альд егид и алког оль), а сама реакция получила название альдольной конденсации, или альдольного присоединения.
Механизм альдольной конденсации. При действии основания в карбонильном соединении отщепляется протон из α-положения и образуется карбанион (I), в котором отрицательный заряд делокализован при участии карбонильной группы.

Анион (I) представляет собой сильный нуклеофил (на следующей стадии механизма он показан цветом), который присоединяется ко второй (неионизированной) молекуле карбонильного соединения. В результате такого взаимодействия возникает новая связь С-С и образуется промежуточный алкоксид-ион (II). В водной среде этот анион стабилизируется, отщепляя протон от молекулы воды, и превращается в конечный продукт - альдоль.

Реакция альдольного присоединения показана на примере пропаналя (цветом выделена молекула, присоединяющаяся к группе С=О другой молекулы); аналогичная реакция приведена на примере ацетона.

Продукт конденсации - альдоль - способен к отщеплению воды с образованием α,β-ненасыщенного карбонильного соединения. Обычно это происходит при повышенной температуре. В этом случае реакция в целом называется кротоновой конденсацией.
Реакции конденсации могут протекать и в смешанном варианте, с использованием разных карбонильных соединений, причем одно из них может и не содержать СН-кислотного центра, как, например, формальдегид и бензальдегид в следующих реакциях:

Альдольная конденсация - обратимая реакция; обратный процесс называется альдольным расщеплением (или ретроальдольной реакцией). Обе реакции происходят во многих биохимических процессах.
5.5. Восстановление и окисление
Восстановление альдегидов и кетонов осуществляют с помощью комплексных гидридов металлов LiAlH 4 , NaBH 4 . Реакция включает нуклеофильную атаку карбонильного атома углерода гидрид-ионом.
При последующем гидролизе образовавшегося алкоголята получается первичный или вторичный спирт.

Окисление альдегидов в карбоновые кислоты осуществляется под действием большинства окислителей, включая кислород воздуха. Кетоны в мягких условиях не окисляются.

Оксид серебра в виде аммиачного комплекса 2 OH (реактив Толленса) окисляет альдегиды в карбоновые кислоты, при этом выделяется металлическое серебро. Отсюда происходит название - реакция «серебряного зеркала».
Так же легко альдегиды окисляются гидроксидом меди(II) в щелочной среде.
Обе эти реакции часто используют как качественные для обнаружения альдегидной группы, хотя они неспецифичны по отношению к альдегидам: окислению указанными реагентами подвергаются, например, многоатомные фенолы, аминофенолы, ароматические амины, гидроксикетоны и другие легкоокисляющиеся соединения.
АЛЬДЕГИДЫ И КЕТОНЫ
Альдегидами и кетонами называют производные углеводородов, содержащие карбонильную группу С=О. В молекуле альдегидов по крайней мере одна валентность карбонильной группы затрачивается на соединение с атомом водорода, а другая - с радикалом (предельного ряда в предельных альдегидах и непредельного - в непредельных альдегидах). Общая формула альдегидов:
причем R может быть равно Н.
В случае кетонов обе валентности карбонильной группы затрачиваются на соединение с радикалами. Общая формула кетонов:
Изомерия. Номенклатура.
Общая формула предельных альдегидов и кетонов С n Н 2 n O.
Изомерия альдегидов связана со строением радикалов. Так, например, известно четыре альдегида с формулой
(см. ниже).
Альдегиды называют или по кислотам, в которые они переходят при окислении (с тем же числом углеродных атомов), или по предельным углеводородам с добавлением суффикса -аль (систематическая номенклатура).
| муравьиный альдегид (формальдегид), метаналь (рис. 1а ) | |
| уксусный альдегид, этаналь (рис. 1б ) | |
| пропионовый альдегид, пропаналь | |
| СН 3 -СН 2 -СН 2 -СНО | масляный альдегид, бутаналь |
| изомасляный альдегид, 2-метилпропаналь | |
| СН 3 -СН 2 -СН 2 -СН 2 -СНО | валериановый альдегид, пентаналь |
| изовалернановый альдегид, 3-метилбутаналь | |
| метилэтилуксусный альдегид, 2-метилбутаналь | |
| триметилуксусный альдегид, 2,2-диметлпропаналь |
Изомерия кетонов связана со строением радикалов и с положением карбонильной группы в углеродной цепи. Кетоны называют по наименованию радикалов, связанных с карбонильной группой. По систематической номенклатуре к названию предельного углеводорода добавляется суффикс -он и указывается номер атома углерода, связанного с карбонильным кислородом:
Способы получения
Альдегиды и кетоны получают рядом общих методов.
1. Окислением или каталитическим дегидрированием первичных спиртов получают альдегиды, вторичных - кетоны. Эти реакции уже приводились при рассмотрении химических свойств спиртов.
2. Альдегиды и кетоны удобно также получать пиролизом кислот и их смесей в виде паров над оксидами некоторых металлов (ThО 2 , МnО 2 , CaO, ZnO) при 400-450 °С:
R - СООН + Н-СООН→R-СНО + СО 2 + Н 2 0
2R-СООН→R -СО -R + C0 2 + Н 2 0
R-СООН + R" - СООН → R - СО-R’+С0 2 + Н 2 0
Во многих учебниках указывается, что альдегиды и кетоны могут быть получены пиролизом Са- и Ва-солей карбоновых кислот. В действительности эта реакция дает очень низкие выходы. Однако некоторые метилкетоны все же могут быть получены пиролизом смесей бариевых или железных солей уксусной и какой-либо другой кислоты. Все эти реакции имеют радикальный механизм.
3. Гидролиз геминальных дигалогенопроизводных приводит к альдегидам, если оба галогена находятся у одного из крайних атомов углерода, и кетонам, если атомы галогена находятся у одного из средних атомов углерода. Эти реакции уже упоминались при изучении химических свойств дигалогенопроизводных углеводородов.
4. Гидратация ацетилена и его гомологов в условиях реакции Кучерова приводит соответственно к уксусному альдегиду или кетонам:
НС≡СН + Н 2 O→ СН 3 -СНО
5. Карбонильные соединения с высокими выходами (порядка 80%) образуются при окислении соответствующих спиртов смесями дпметилсульфоксида с уксусным ангидридом или безводной фосфорной кислотой.
RCH 2 OH + (CH 3) 2 SO→ RCH = О + (CH 3) 2 S
6. Превращение галогеналкилов в альдегиды с удлинением цепи на один атом углерода достигается обработкой их натрийтетракарбонилферратом в присутствии трифенилфосфина, а затем уксусной кислотой:
R - Hlg + Na 2 Fe(CO) 4 RCOFe(CO 3)P(C 6 H 5) 3 R–CH = О
Имеется несколько модификаций этого метода.
7. Кетоны с хорошими выходами получаются при взаимодействии хлорангидридов кислот с литийдиалкилкупратамн и кадмийалкилами:
R 2 CuLi + R"COCI→R - СО - R"+LiCI + R - Сu
8. В технике альдегиды получают прямым присоединением СО и H 2 к олефинам (оксосинтез) при 100-200 °С под давлением 10-20 МПа (100-200 атм) в присутствии кобальтового или никелевого катализаторов (например, Со + ThO 2 + MgO, нанесенные на кизельгур):
Реакцию с этиленом и пропиленом проводят в газовой фазе, а с более сложными олефинамн (С 4 -С 20) - в жидкой фазе. Как видно из приведенной схемы, при оксосинтезе получаются альдегиды, содержащие на один атом углерода больше, чем исходные олефины. Этот синтез имеет важное значение для получения высших первичных спиртов (каталитическим восстановлением альдегидов). Механизм оксосинтеза можно представить следующим образом:
2Со + 8СО→ Со 2 (СО) 8
Cо 2 (CO)8 + H 2 → 2НСо(СО) 4
R -СН=СН 2 + НСо(СО) 4 → R - СН 2 -СН 2 - Со(СО) 4
R - СН 2 -СН 2 -Со(СО) 4 +СО→ R-СН 2 -СН 2 -СО - Со(СО) 4
R-СН 2 -СН 2 -СО-Со(СО) 4 + НСо(СО) 4 →R-СН 2 -СН 2 -СНО + Со(СО) 8
Физические свойства
Муравьиный альдегид - газ с весьма резким запахом. Другие низшие альдегиды и кетоны - жидкости, легко растворимые в воде; низшие альдегиды обладают удушливым запахом, который при сильном разведении становится приятным (напоминает запах плодов). Кетоны пахнут довольно приятно.
При одном и том же составе, и строении углеродной цепи кетоны кипят при несколько более высоких температурах, чем альдегиды. Температуры кипения альдегидов и кетонов с нормальным строением цепи выше, чем у соединений изостроения. Например, валериановый альдегид кипит при 103,4 °С, а изовалериановый - при 92,5 °С. Альдегиды и кетоны кипят при температуре, значительно более низкой, чем спирты с тем же числом углеродных атомов, например у пропионового альдегида т. кип. 48,8 °С, у ацетона 65,1 °С, у н -пропилового спирта 97,8 °С. Это показывает, что альдегиды и кетоны в отличие от спиртов не являются сильно ассоциированными жидкостями. В то же время температуры кипения карбонильных соединений значительно выше температур кипения углеводородов с той же молекулярной массой, что связано с их высокой полярностью. Плотность альдегидов и кетонов ниже единицы.
В ИК-спектрах для СО-группы характерно интенсивное поглощение при 1720 см -1 . В спектре ЯМР сигнал водорода альдегидной группы находится в очень слабом поле.
Химические свойства
Альдегиды и кетоны отличаются большой реакционной способностью. Большинство их реакций обусловлено присутствием активной карбонильной группы. Двойная связь карбонильной группы сходна по физической природе с двойной связью между двумя углеродными атомами (σ-связь + π-связь). Однако в то время как Е с=с <2Е с-с, энергия связи С=О (749,4 кДж/моль) больше, чем энергия двух простых С-О-связей (2х358 кДж/моль). С другой стороны, кислород является более электроотрицательным элементом, чем углерод, и потому электронная плотность вблизи атома кислорода больше, чем вблизи атома углерода. Дипольный момент карбонильной группы - около 9 10 -30 Кл/м (2,7 D). Благодаря такой поляризации углеродный атом карбонильной группы обладает электрофильными свойствами и способен реагировать с нуклеофильными реагентами. Соответственно атом кислорода является нуклеофильным. В реакциях присоединения отрицательно поляризованная часть присоединяющейся молекулы всегда направляется к углеродному атому карбонильной группы, в то время как ее положительно поляризованная часть направляется к кислородному атому.
Реакция присоединения нуклеофильных реагентов по месту карбонильной связи - ступенчатый процесс. Схематически реакцию присоединения, например гидросульфита натрия к уксусному альдегиду, можно изобразить следующим образом:
Радикалы, способные увеличивать положительный заряд на атоме углерода карбонильной группы, сильно повышают реакционную способность альдегидов и кетонов; радикалы или атомы, уменьшающие положительный заряд на этом углеродном атоме, оказывают противоположное действие.
Помимо реакций присоединения по карбонильной группе для альдегидов и кетонов характерны также реакции с участием соседних с карбонильной группой углеродных радикалов, обусловленные электроноакцепторным влиянием на них карбонильной группы. К ним относятся реакции окисления, галогенирования, конденсации.
А. Гидрирование. Присоединение водорода к альдегидам и кетонам происходит в присутствии катализаторов гидрирования (Ni, Со, Си, Pt, Pd и др.). При этом альдегиды переходят в первичные, а кетоны - во вторичные спирты. На этом основан один из методов получения спиртов.
В последнее время в качестве восстанавливающего агента часто применяют лнтийалюминийгидрид LiА1Н 4 . Реакция идет с переносом гидридного иона:
Преимуществом восстановления с помощью LiAlН 4 является то, что этот реагент не восстанавливает двойные углерод-углеродные связи.
При восстановлении альдегидов или кетонов водородом в момент выделения (с помощью щелочных металлов или амальгамированного магния) образуются наряду с соответствующими спиртами также гликоли:
пинакон
Соотношение между образующимися спиртом и гликолем зависит от природы карбонильного соединения и условий восстановления. При восстановлении кетонов в продуктах реакции в апротонных растворителях преобладают пинаконы; в случае алифатических насыщенных альдегидов гликоли образуются в малых количествах.
Реакция протекает с промежуточным образованием свободных радикалов:
Б. Реакции нуклеофильного присоединения.
1. Присоединение магнийгалогеналкилов подробно разобрано при описании методов получения спиртов.
2. Присоединение синильной кислоты приводит к образованию α-оксинитрилов, омылением которых получают α-гидроксикислоты:
нитрил α-гидроксипропионовой кислоты
Эта реакция начинается нуклеофильной атакой углеродного атома ионом CN - . Цианистый водород присоединяется очень медленно. Добавление капли раствора цианистого калия значительно ускоряет реакцию, в то время как добавление минеральной кислоты уменьшает скорость реакции практически до нуля. Это показывает, что активным реагентом при образовании циангидрина является ион CN - :
3. Присоединение гидросульфита натрия дает кристаллические вещества, обычно называемые гидросульфитными производными альдегидов или кетонов:
При нагревании с раствором соды или минеральных кислот гидросульфитные производные разлагаются с выделением свободного альдегида или кетона, например:
Реакция с гидросульфитом натрия используется для качественного определения альдегидов и кетонов, а также для их выделения и очистки. Следует, однако, заметить, что в реакцию с гидросульфитом натрия в жирном ряду вступают только метилкетоны, имеющие группировку СН 3 -СО- .
4. Взаимодействие с аммиаком позволяет различать альдегиды и кетоны. Альдегиды выделяют воду, образуя альдимины:
ацетальдимин, этаними н
которые легко полимеризуются (циклизуются в кристаллические тримеры - альдегидаммиаки:
альдегидаммиа к
При циклизации разрывается двойная связь C = N и три молекулы имина соединяются в шестичленный цикл с чередующимися атомами углерода и азота.
Кетоны с аммиаком подобных соединений не образуют. Они реагируют очень медленно и более сложно, например, так:
5. С гидроксиламином альдегиды и кетоны, выделяя воду, образуют оксимы (альдоксимы и кетоксимы):
ацетальдоксим
ацетоноксим
Эти реакции применяют для количественного определения карбонильных соединений.
Механизм реакции (R=H или Alk):
6. Особый интерес представляют реакции карбонильных соединений с гидразином и его замещенными. В зависимости от условий гидразин вступает в реакцию с альдегидами и кетонами в соотношении 1:1 или 1:2. В первом случае образуются гидразоны, а во втором - азины (альдазины и кетазины):
гидразон
альдазин
кетазин
Гидразоны кетонов и альдегидов при нагревании с твердым КОН выделяют азот и дают предельные углеводороды (реакция Кижнера):
В настоящее время эту реакцию проводят нагреванием карбонильного соединения с гидразином в высококипящих полярных растворителях (ди- и триэтиленгликоли) в присутствии щелочи. Реакция может быть проведена и при комнатной температуре при действии трет-бутилкалия в диметлисульфоксиде.
Альдегиды и кетоны с замещенными гидразинами - с фенилгидразином C 6 H 5 -NH-NH 2 и семикарбазидом образуют соответственно фенилгидразоны и семикарбазоны. Это кристаллические вещества. Они служат для качественного и количественного определения карбонильных соединений, а также для их выделения и очистки.
Образование фенилгидразонов:
Семикарбазоны образуются по схеме:
Реакции альдегидов и кетонов с производными гидразина по механизму аналогичны их реакциям с аммиаком и гидроксиламином. Например, для ацетальдегида и фенилгидразина:
Для этих реакций характерен кислотный катализ.
7. Альдегиды и кетоны способны присоединять по карбонильной группе воду с образованием гидратов - геминальных гликолей. Эти соединения во многих случаях существуют только в растворах. Положение равновесия зависит от строения карбонилсодержащего соединения:
Так, формальдегид при 20 °С существует в водном растворе на 99,99% в форме гидрата, ацетальдегид- на 58%; в случае ацетона содержание гидрата незначительно, а хлораль и трихлорацетон образуют стойкие кристаллические гидраты.
Альдегиды с более высокой молекулярной массой образуют с водой устойчивые при низких температурах твердые полугидраты:
8.
В присутствии следов минеральной кислоты образуются ацетали:
Ацетали - жидкости с приятным эфирным запахом. При нагревании с разбавленными минеральными кислотами (но не щелочами) они подвергаются гидролизу с образованием спиртов и выделением альдегидов:
Ацеталь, полученный из масляного альдегида и поливинилового спирта, используется в качестве клея при изготовлении безосколочных стекол.
Ацетали кетонов получаются более сложно - действием на кетоны этиловых эфиров ортомуравьиной НС(ОС2Н 5)з или ортокремниевой кислоты:
9. При действии на альдегиды спиртов образуются полуацетали:
Альдегиды и кетоны при взаимодействии с PCI 5 обменивают атом кислорода на два атома хлора, что используется для получения геминаль- ных дихлоралканов:
Эта реакция в стадии, определяющей характер конечного продукта, также является реакцией нуклеофильного присоединения:
В. Реакции окисления. Окисление альдегидов идет значительно легче, чем кетонов. Кроме того, окисление альдегидов приводит к образованию кислот без изменения углеродного скелета, в то время как кетоны окисляются с образованием двух более простых кислот или кислоты и кетона.
Альдегиды окисляются кислородом воздуха до карбоновых кислот. Промежуточными продуктами являются гидропероксиды:
Аммиачный раствор гидроксида серебра OH при легком нагревании с альдегидами (но не с кетонами) окисляет их в кислоты с образованием свободного металлического серебра. Если пробирка, в которой идет реакция, была предварительно обезжирена изнутри, то серебро ложится тонким слоем на ее внутренней поверхности - образуется серебряное зеркало:
Эта реакция, известная под названием реакции серебряного зеркала, служит для качественного определения альдегидов.
Для альдегидов характерна также реакция с так называемой фелинговой жидкостью. Последняя представляет собой водно-щелочной раствор комплексной соли, образовавшейся из гидроксида меди и натрийкалиевой соли винной кислоты. При нагревании альдегидов с фелинговой жидкостью медь (II) восстанавливается до меди (I), а альдегид окисляется до кислоты:
Красная окись меди Cu 2 О почти количественно выпадает в осадок. Реакция эта с кетонами не идет.
Альдегиды могут быть окислены в карбоновые кислоты с помощью многих обычных окислителей, таких, как дихромат калия, перманганат калия, по ионному механизму, причем первой стадией процесса обычно является присоединение окислителя по СО-группе.
Окисление кетонов протекает с разрывом углеродной цепочки в разных направлениях в зависимости от строения кетонов.
По продуктам окисления можно судить о строении кетонов, а так как кетоны образуются при окислении вторичных спиртов, то, следовательно, и о строении этих спиртов.
Г. Реакции полимеризации. Эти реакции характерны только для альдегидов. При действии на альдегиды кислот происходит их тримеризация (частично и тетрамеризация):
Механизм полимеризации может быть представлен в следующем виде:
Д. Галогенирование. Альдегиды и кетоны реагируют с бромом и иодом с одинаковой скоростью независимо от концентрации галогена. Реакции ускоряются как кислотами, так и основаниями.
Подробное изучение этих реакций привело к выводу, что они идут с предварительным превращением карбонильного соединения в енол:
Е. Реакции конденсации.
1. Альдегиды в слабоосновной среде (в присутствии ацетата, карбоната или сульфита калия) подвергаются альдольной конденсации (А.П. Бородин) с образованием альдегидосииртов (гидроксиальдегидов), сокращенно называемых альдолями. Альдоли образуются в результате присоединения альдегида к карбонильной группе другой молекулы альдегида с разрывом связи С-Н в α-положении к карбонилу, как это показано на примере уксусного альдегида:
альдоль
В случае альдолизацин других альдегидов, например пропионового, в реакцию вступает только группа, находящаяся в a-положении к карбонилу, так как только водородные атомы этой группы в достаточной степени активируются карбонильной группой:
3-гидрокси-2-метилпентаналь
Если рядом с карбонилом находится четвертичный атом углерода, альдолизация невозможна. Например, триметилуксусный альдегид (СНз)зС-СНО не дает альдоля.
Механизм реакции альдольной конденсации, катализируемой основаниями, следующий. Альдегид проявляет свойства СН-кислоты. Гидроксильный ион (катализатор) обратимо отрывает протон от а-углеродного атома:
Альдоль при нагревании (без водоотнимающих веществ) отщепляет воду с образованием непредельного кротонового альдегида:
Поэтому переход от предельного альдегида к непредельному через альдоль называется кротоновой конденсацией. Дегидратация происходит благодаря очень большой подвижности водородных атомов в α-положении по отношению к карбонильной группе (сверхсопряжение), причем разрывается, как и во многих других случаях, p-связь по отношению к карбонильной группе.
При действии на альдегиды, способные к альдольной конденсации, сильных оснований (щелочей) в результате глубокой альдольной (или кротоновой) поликонденсации происходит осмоление. Альдегиды, не способные к альдольной конденсации, в этих условиях вступают в реакцию Канниццаро:
2(СН 3) 3 С-СНО +КОН→(СН 3) 3 С-COOK +(СН 3) 3 С-СН 2 ОН.
Альдольная конденсация кетонов происходит в более жестких условиях - в присутствии оснований, например Ва(ОН) 2 . При этом образуются Р-кетоноспирты, легко теряющие молекулу воды:
В еще более жестких условиях, например при нагревании с концентрированной серной кислотой, кетоны подвергаются межмолекулярной дегидратации с образованием непредельных кетонов:
окись мезитила
Окись мезитила может реагировать с новой молекулой ацетона:
форон
Возможна и конденсация между альдегидами и кетонами, например:
3-пентен-2-он
Во всех этих реакциях вначале идет альдольная конденсация, а затем дегидратация образовавшегося гидроксикетона.
2. Сложноэфирная конденсация альдегидов проходит при действии на них алкгоголятов алюминия в неводной среде (В.Е. Тищенко).
уксусноэтиловый эфир
Ж. Декарбонилирование. Альдегиды при нагревании с трис(трифенилфосфин)родийхлоридом претерпевают декарбонилирование с образованием углеводородов:
R-СНО + [(C 6 H 5) 3 P] 3 PhCl→ R-Н + [(C 6 H 5) 3 P] 3 RhCOCl.
При изучении химических превращений альдегидов и кетонов необходимо обратить внимание на существенные различия между ними. Альдегиды легко окисляются без изменения углеродной цепи (реакция серебряного зеркала), кетоны окисляются трудно с разрывом цепи. Альдегиды полимеризуются под влиянием кислот, образуют альдегидоаммиаки, со спиртами в присутствии кислот дают ацетали, вступают в сложноэфирную конденсацию, дают окрашивание с фуксинсернистой кислотой. Кетоны не способны к подобным превращениям.
Отдельные представители. Применение
Муравьиный альдегид (формальдегид) - бесцветный газ с резким специфическим запахом, т. кип. -21 °С. Он ядовит, действует раздражающе на слизистые оболочки глаз и дыхательных путей. Хорошо растворим в воде, 40% -ный водный раствор формальдегида называется формалином. В промышленности формальдегид получают двумя методами - неполным окислением метана и его некоторых гомологов и каталитическим окислением или дегидрированием метанола (при 650-700 °С над серебряным катализатором):
СН 3 ОН→ Н 2 +Н 2 СО.
Благодаря отсутствию алкильного радикала формальдегиду присущи некоторые особые свойства.
1. В щелочной среде он претерпевает реакцию окисления - восстановления (реакция Канниццаро):
2. При легком нагревании формальдегида (формалина) с аммиаком получается гексаметилентетрамин (уротропин), синтезированный впервые А. М. Бутлеровым:
6Н 2 С=О + 4NH 3 → 6H 2 0 + (CH 2) 6 N 4
уротропин
Уротропин в больших количествах применяют в производстве фенолформальдегидных смол, взрывчатых веществ (гексогена, получаемого нитрованием уротропина)
гексаген
в медицине (в качестве мочегонного средства, как составная часть антигриппозного препарата кальцекса, при лечении почечных заболеваний и др.).
3. В щелочной среде, например в присутствии известкового молока, как это впервые было показано А. М. Бутлеровым, формальдегид подвергается альдолизации с образованием оксиальдегидов вплоть до гексоз и еще более сложных сахаров, например:
гексоза
В присутствии щелочей формальдегид может конденсироваться и с другими альдегидами, образуя многоатомные спирты. Так, конденсацией формальдегида с уксусным альдегидом получают четырехатомный спирт - пентаэритрит С(СН 2 ОН) 4
СН 3 СНО + 3Н 2 СО → (НОСН 2) 3 ССНО
(НОСН 2) 3 ССНО + Н 2 СО → (НОСН 2) 4 С + НСОО -
Пентаэритрит используется для получения смол и весьма сильного взрывчатого вещества - тетранитропентаэритрита (ТЭН) C(CH 2 ОNО 2) 4 .
4. Формальдегид способен к полимеризации с образованием циклических и линейных полимеров.
5. Формальдегид способен вступать в различные реакции конденсации с образованием синтетических смол, широко применяемых в промышленности. Так, поликонденсацией формальдегида с фенолом получают фенолформальдегидные смолы, с мочевиной или меламином - карбамидные смолы.
6. Продуктом конденсации формальдегида с изобутиленом (в присутствии H 2 SO 4) является 4,4-диметил-1,3-диоксан, который при нагревании до 200-240 °С в присутствии катализаторов (SiO 2 +Н 4 Р 2 О 7) разлагается с образованием изопрена.
Формалин широко применяется в качестве дезинфицирующего вещества для дезинфекции зерно- и овощехранилищ, парников, теплиц, для протравливания семян и т. д.
Уксусный альдегид, ацетальдегид СН 3 СНО - жидкость с резким неприятным запахом. Т.кип. 21 °С. Пары ацетальдегида вызывают раздражение слизистых оболочек, удушье, головную боль. Ацетальдегид хорошо растворим в воде и во многих органических растворителях.
Промышленные методы получения ацетальдегида уже были рассмотрены: гидратация ацетилена, дегидрирование этилового спирта, изомеризация окиси этилена, каталитическое окисление воздухом предельных углеводородов.
В последнее время ацетальдегид получают окислением этилена кислородом воздуха в присутствии катализатора по схеме:
CH 2 =CH 2 +H 2 O +PdCl 2 →CH 3 -СНО + 2HCl + Pd
Pd + 2CuC1 2 → 2CuCl + PdCl 2
2CuCl + 2HCI + 1 / 2 O 2 → 2CuCI 2 + H 2 O
2CH 2 = CH 2 + O 2 →2CH 3 CHO
Другие 1-алкены образуют в этой реакции метилкетоны.
Из ацетальдегида в промышленных масштабах получают уксусную кислоту, уксусный ангидрид, этиловый спирт, альдоль, бутиловый спирт, ацетали, этилацетат, пентаэритрит и ряд других веществ.
Подобно формальдегиду, он конденсируется с фенолом, аминами и другими веществами, образуя синтетические смолы, которые используются в производстве различных полимерных материалов.
Под действием небольшого количества серной кислоты ацетальдегид полимеризуется в паральдегид (С 2 Н 4 О 3) 3 и метальдегид (С 2 Н 4 О 3) 4 ; количества последнего возрастают с понижением температуры (до -10 °С):
Паральдегид - жидкость с т. кип. 124,5 °С, метальдегид - кристаллическое вещество. При нагревании со следами кислоты оба эти вещества деполимеризуются, образуя ацетальдегид. Из паральдегида и аммиака получают 2-метил-5-винилпиридин, используемый при синтезе сополимеров - синтетических каучуков.
Трихлоруксусный альдегид, хлораль CCI 3 CHO, получают хлорированием этилового спирта.
Хлораль - бесцветная жидкость с резким запахом; с водой образует кристаллический гидрат - хлоральгидрат. Устойчивость хлоральгидрата объясняется усилением электроноакцепторных свойств карбонильного углерода под влиянием сильного индукционного эффекта хлора:
Обладает снотворным действием. Конденсацией хлораля с хлорбензолом получают в промышленных масштабах инсектициды.
При действии на хлораль щелочей образуется хлороформ:
Ацетон СН 3 СОСН 3 - бесцветная жидкость с характерным запахом; Т.кип.=56,1 °С, Т.пл.=0,798. Хорошо растворим в воде и во многих органических растворителях.
Ацетон получают:
1) из изопропилового спирта - окислением или дегидрированием;
2) окислением изопропилбензола, получаемого алкилированием бензола, наряду с фенолом;
3) ацетон-бутанольным брожением углеводов.
Ацетон в качестве растворителя применяется в больших количествах в лакокрасочной промышленности, в производствах ацетатного шелка, кинопленки, бездымного пороха (пироксилина), для растворения ацетилена (в баллонах) и т. д. Он служит исходным продуктом при производстве небьющегося органического стекла, кетена и т. д.
Номенклатура
Альдегиды суффикс аль

Кетоны суффикс он

Методы получения
1. Гидратация алкинов (реакция Кучерова) (см. тему “Алкины”)
2. Окисление и дегидрирование первичных и вторичных спиртов (см. тему “Спирты”)
3. Пиролиз (декарбоксилирование) солей карбоновых кислот

Реакционная способность

Атомы углерода и кислорода в карбонильной группе находятся в sp 2 -гибридизации, группа имеет плоское строение. Связь СО поляризована, электронная плотность смещена к атому кислорода.

Дефицит электронной плотности на атоме углерода карбонила (+d ") в кетонах меньше, чем в альдегидах (+d) из-за донорных эффектов двух алкильных групп. Следствием этого является снижение реакционной способности карбонильной группы в кетонах.
I. Реакции присоединения по карбонильной группе
1. Восстановление (гидрирование) – синтезпервичных и вторичных спиртов.
При восстановлении или гидрировании альдегидов получают первичные спирты, из кетонов образуются вторичные спирты.
а) гидрирование

б) восстановление боргидридом натрия (NaBH 4) и алюмогидридом лития (LiAlH 4)

2. Присоединение HCN – образование циангидринов или нитрилов 2-оксикислот.
Реакция носит название циангидринного синтеза и используется при получении 2-окси- и 2-аминокислот (см. материалы 2-го семестра).

Механизм Ad Nu –нуклеофильное присоединение по карбонильной группе
Nu – − :С≡N (нитрил-анион)
В качестве реагента также можно использовать КСN в присутствии воды.

2. Присоединение NaHSO 3 (гидросульфита натрия) – образование бисульфитного производного (качественная реакция )

Механизм Ad Nu , Nu –атом серы за счет НПЭ:
Пространственно затрудненные (разветвленные) кетоны, например диизопропилкетон, не образуют бисульфитные производные. Реакция может служить качественной, бисульфитные производные легко кристаллизуются. Эту реакцию также используют для выделения альдегидов (кетонов) из смеси с другими соединениями.
4. Присоединение реактивов Гриньяра – синтез спиртов всех типов.
а) из формальдегида получают первичные спирты

б) из других альдегидов получают вторичные спирты
в) из кетонов получают третичные спирты

Присоединение слабых нуклеофилов
Для присоединения слабых нуклеофилов необходим кислый катализ.
1. Присоединение H 2 O , НХ Х=Cl, Br
Реакции с этими реагентами обратимы, продукты присоединения (аддукты) нестабильны.

Исключением являются аддукты воды и альдегидов (кетонов), имеющих акцепторные группы.

2. Присоединение спиртов – образование полуацеталей (полукеталей), ацеталей (кеталей).
Присоединение одной молекулы спирта к альдегиду приводит к синтезу полуацеталей, к кетону – полукеталей. При дальнейшем взаимодействии со второй молекулой спирта из полуцеталя образуется ацеталь, из полукеталя – кеталь. Полуацетали и полукетали содержат при одном атоме углерода гидроксильную и алкоксигруппы, у ацеталей и кеталей – при одном атоме углерода две алкоксигруппы.

Механизм образования полуацеталя и ацеталя приведен ниже:

II. Реакции присоединения-отщепления (реакции с азотистыми нуклеофилами).
Реакции с соединениями с общей формулой NH 2 -X, где Х = H, OH, NH 2 , NH-C 6 H 5 , NH-C(O)NH 2 , NH-C 6 H 3 (о, п-NO 2) идут в два этапа, промежуточные аддукты нестабильны.
Общая схема реакции:

1. Реакция с аммиаком – образование иминов.

Альдимины нестойки и вступают в реакции циклизации:

При взаимодействии 6 молей формальдегида и 4 молей аммиака образуется уротропин (гексаметилентетрамин), впервые синтезированный А. М. Бутлеровым в 1859 году. Уротропин используется для лечения мочевыводящих путей, его комплекс с хлористым кальцием называется кальцексом и применятся в качестве антигриппозного средства.

2. Реакция с гидроксиламином - NH 2 OH – образование оксимов.

Реакция относится к качественным. Оксимы – кристаллические вещества, легко кристаллизуются.
3. Реакции с гидразином – NH 2 - NH 2 , фенилгидразином - NH 2 - NH - C 6 H 5 и с 2,4-динитрофенилгидразином - NH 2 - NH - C 6 H 3 -2,4-(NO 2) 2 – образование гидразонов, фенилгидразонов и 2,4-динитрофенилгидразонов.

По аналогичной схеме образуются фенилгидразоны и 2,4-динитрофенилгидразоны:

2,4-Динитрофенилгидразоны особенно широко используются для идентификации альдегидов и кетонов. Они обладают высокими температурами плавления, легко кристаллизуются, имеют четкие спектральные данные.
3. Реакция с семикарбазидом – NH 2 - NH - CONH 2 – образование семикарбазонов.

Все выше описанные реакции катализируются слабыми кислотами, в случае реакции с 2,4-динитрофенилгидразином реакция идет в присутствии концентрированной серной кислоты. Механизм однотипен – нуклеофильное присоединение-отщепление и описан ниже в общем виде:

Х=H, OH, NH 2 , NH-C 6 H 5 , NH-C(O)NH 2
Получаемые имино-производные при кислом или щелочном гидролизе дают исходные альдегиды (кетоны).
III. Реакции с участием атомов водорода при a -углеродном атоме
Для альдегидов и кетонов, имеющих атомы водорода в a-положение характерно явление таутомерии.
Таутомерия – это процесс динамической изомеризации. Структурные изомеры (в данном случае таутомеры), взаимно превращаясь, находятся в состоянии динамического равновесия. Как правило, при изомеризации происходит перенос протона, в этом случае таутомерию называют прототропной.

При наличии двух a-положений в кетонах возможно образование двух енолов.
Альдегиды и кетоны образуются через енолы при гидратации алкинов по реакции Кучерова (см. тему «Алкины»). Енолы или енолят-анионы являются промежуточными соединениями в реакциях галоидирования и конденсации карбонильных соединений.
1. Галоидирование карбонильных соединений (идет только по α-положению).
а) Хлорирование
Хлорирование хлором идет без катализатора, результат зависит от количества хлора, можно получить моно, ди и трихлорпроизводные (для этаналя).

б) Бромирование

Хлорирование идет легко и без катализатора, в зависимости от количества реагента и строения соединения можно ввести от одного до трех атомов хлора. При бромировании используют 1 моль реагента в присутствии щелочи.
в) Галоформное расщепление (изб. I 2 , Cl 2 или Br 2 , Na ОН (конц.))
Качественная реакция на наличие ацетильного фрагмента (СН 3 СО) в карбонильных соединениях. При реакции с йодом и бромом выпадает окрашенный осадок галоформа, обладающий специфическим запахом.

Механизм реакции

Галоформному расщеплению подвергаются ацетальдегид и метилалкилкетоны, при этом кроме галоформа в реакции образуются натриевые соли карбоновых кислот.
2. Реакции альдольной и кротоновой конденсации
Конденсация – это реакция, приводящая к усложнению углеводородного скелета. В альдольной и кротоновой конденсациях участвуют две молекулы карбонильного соединения. Одна молекула – карбонильная компонента , реагирует с помощью карбонильной группы, другая – метиленовая компонента за счет атомов водорода α-положения.
а) Альдольная конденсация (реакция катализируется основаниями)

Механизм Ad Nu

Альдоли способны при нагревании в щелочной среде отщеплять воду и превращаться в a,b - непредельные альдегиды (кетоны).

б) Кротоновая конденсация (в кислой среде при нагревании). Протекает по механизму Аd E .

В кислой среде при нагревании конденсация не останавливается на стадии образования альдоля. Происходит внутримолекулярная дегидратация альдоля до непредельного альдегида или кетона. При участии в реакции пропаналя, бутаналя и других альдегидов получают альдегиды и кетоны, имеющие в положении С-2 алкильную группу.

Механизм Ad Е

IV. Реакции окисления
1. Альдегиды окисляются в мягких условиях до карбоновых кислот, проявляя свойства восстановителей.

Реакции с растворами Толенса (реакция серебряного зеркала) и Фелинга относятся к качественным.
2. Кетоны окисляются деструктивно с расщеплением молекулы в жестких условиях после енолизации под действием KMnO 4 и K 2 Cr 2 O 7 в присутствии концентрированной серной кислоты (реакцию не описываем).
Лекция № 11
АЛЬДЕГИДЫ И КЕТОНЫ
План
1. Методы получения.
2. Химические свойства.
2.1. Реакции нуклеофильного
присоединения.
2.2. Реакции по a -углеродному атому.
2.3.
Лекция № 11
АЛЬДЕГИДЫ И КЕТОНЫ
План
1. Методы получения.
2. Химические свойства.
2.1. Реакции нуклеофильного
присоединения.
2.2. Реакции по a -углеродному атому.
2.3. Реакции окисления и восстановления.
Альдегиды и кетоны содержат карбонильную группу
С=О. Общая формула:
1. Методы получения.

2. Химические
свойства.
Альдегиды и кетоны – один из наиболее реакционноспособных классов
органических соединений. Их химические свойства определяются присутствием
карбонильной группы. Вследствие большого различия в электроотрицательностях
углерода и кислорода и высокой поляризуемости p
-связи связь С=О обладает значительной полярностью
(m
С=О
=2,5-2,8 D). Атом углерода карбонильной
группы несет эффективный положительный заряд и является объектом для атаки
нуклеофилов. Основной тип реакций альдегидов и кетонов – реакции
нуклеофильного присоединения Ad
N . Кроме того, карбонильная группа оказывает влияние на
реакционную способность связи С-Н в
a
-положении, повышая ее кислотность.
Таким образом, молекулы альдегидов и кетонов
содержат два основных реакционных центра – связь С=О и связь С-Н в
a
-положении:

2.1. Реакции нуклеофильного
присоединения.
Альдегиды и кетоны легко присоединяют нуклеофильные реагенты по С=О связи.
Процесс начинается с атаки нуклеофила по карбонильному атому углерода. Затем
образующийся на первой стадии тетраэдрический интермедиат присоединяет протон и
дает продукт присоединения:

Активность карбонильных соединений в
Ad
N –реакциях зависит от величины
эффективного положительного заряда на карбонильном атоме углерода и объема
заместителей у карбонильной группы. Электронодонорные и объемистые заместители
затрудняют реакцию, электроноакцепторные заместители повышают реакционную
способность карбонильного соединения. Поэтому альдегиды в
Ad
N –реакциях активнее, чем
кетоны.
Активность карбонильных соединений повышается в
присутствии кислотных катализаторов, которые увеличивают положительный заряд на
карбонильном атоме углерода:

Альдегиды и кетоны присоединяют воду, спирты,
тиолы, синильную кислоту, гидросульфит натрия, соединения типа
NH
2 X. Все реакции присоединения
идут быстро, в мягких условиях, однако образующиеся продукты, как правило,
термодинамически не устойчивы. Поэтому реакции протекают обратимо, и содержание
продуктов присоединения в равновесной смеси может быть низким.
Присоединение воды.
Альдегиды и кетоны присоединяют воду с
образованием гидратов. Реакция протекает обратимо. Образующиеся гидраты
термодинамически не стабильны. Равновесие смещено в сторону продуктов
присоединения только в случае активных карбонильных соединений.

Продукт гидратации трихлоруксусного альдегида
хлоральгидрат – устойчивое кристаллическое соединение, которое используется в
медицине как успокаивающее и снотворное средство.
Присоединение спиртов и
тиолов.
Альдегиды присоединяют спирты с образованием полуацеталей
. При избытке спирта и в присутствии кислотного катализатора
реакция идет дальше – до образования ацеталей

Реакция образования полуацеталя протекает как
нуклеофильное присоединение и ускоряется в присутствии кислот или
оснований.

Процесс образования ацеталя идет как
нуклеофильное замещение ОН группы в полуацетале и возможен только в условиях
кислотного катализа, когда группа ОН превращается в хорошую уходящую группу
(H
2 O).

Образование ацеталей – обратимый процесс. В
кислой среде полуацетали и ацетали легко гидролизуются. В щелочной среде
гидролиз не идет. Реакции образования и гидролиза ацеталей играют важную роль в
химии углеводов.
Кетоны в аналогичных условиях кеталей не
дают.
Тиолы как более сильные нуклеофилы, чем спирты,
образуют продукты присоединения и с альдегидами, и с кетонами.
Присоединение синильной
кислоты
Синильная кислота присоединяется к карбонильным соединением в условиях
основного катализа с образованием циангидринов.

Реакция имеет препаративное значение и
используется в синтезе
a
-гидрокси- и
a
-аминокислот (см. лек. № 14). Плоды некоторых растений
(например, горький миндаль) содержат циангидрины. Выделяющаяся при их
расщеплении синильная кислота оказывает отравляющее действие
.
Присоединение бисульфита
натрия.
Альдегиды и метилкетоны присоединяют бисульфит натрия NaHSO 3 c образованием бисульфитных производных.

Бисульфитные производные карбонильных соединений
– кристаллические вещества, не растворимые в избытке раствора бисульфита натрия.
Реакция используется выделения карбонильных соединений из смесей. Карбонильное
соединение может быть легко регенерировано обработкой бисульфитного производного
кислотой
или щелочью.
Взаимодействие с соединениями общей
формулы NH
2 X.
Реакции протекают по общей схеме как процесс
присоединения-отщепления. Образующийся на первой стадии продукт присоединения не
устойчив и легко отщепляет воду.

По приведенной схеме с карбонильными
соединениями реагируют аммиак, первичные амины, гидразин, замещенные гидразины,
гидроксиламин.

Образующиеся производные представляют собой
кристаллические вещества, которые используют для выделения и идентификации
карбонильных соединений.
Имины (основания Шиффа) являются промежуточными
продуктами во многих ферментативных процессах (трансаминирование под действием
кофермента пиридоксальфосфата; восстановительное аминирование кетокислот при
участии кофермента НАД
Н). При каталитическом гидрировании иминов образуются
амины. Процесс используется для синтеза аминов из альдегидов и кетонов и
называется восстановительным аминированием.
Восстановительное аминирование протекает in vivo
в ходе синтеза аминокислот (см. лек. № 16)
2.2. Реакции по a -углеродному атому.
Кето-енольная таутомерия.
Водород в
a
-положении к карбонильной группе обладает кислотными
свойствами, так как образующийся при его отщеплении анион стабилизируется за
счет резонанса.

Результатом протонной подвижности атома водорода
в
a
-положении
является способность карбонильных соединений к образованию енольных форм за счет
миграции протона из
a
-положения к атому кислорода карбонильной группы.

Кетон и енол являются таутомерами
.
Таутомеры – это изомеры, способные быстро и обратимо превращаться друг в друга
за счет миграции какой-либо группы (в данном случае – протона). Равновесие между
кетоном и енолом называют кето-енольной таутомерией.
Процесс енолизации катализируется кислотами и
основаниями. Енолизация под действием основания может быть представлена
следующей схемой:
Большинство карбонильных соединений существуют
преимущественно в кетонной форме. Содержание енольной формы возрастает с
увеличением кислотности карбонильного соединения, а также в случае
дополнительной стабилизации енольной формы за счет водородной связи или за счет
сопряжения.
Таблица 8. Содержание енольных форм и
кислотность карбонильных соединений
Например, в 1,3-дикарбонильных соединениях
подвижность протонов метиленовой группы резко увеличивается за счет
электроноакцепторного влияния двух карбонильных групп. Кроме того, енольная
форма стабилизируется за счет наличия в ней системы сопряженных
p
-связей и внутримолекулярной
водородной связи.

Если соединение в енольной форме представляет
собой сопряженную систему с высокой энергией стабилизации, то енольная форма
преобладает. Например, фенол существует только в енольной форме.
Енолизация и образование енолят-анионов являются
первыми стадиями реакций карбонильных соединений, протекающих по
a
-углеродному атому. Важнейшими
из них являются галогенирование
и альдольно-кротоновая
конденсация
.
Галогенирование.
Альдегиды и кетоны легко вступают в реакцию с галогенами (Cl 2 ,
Br 2 , I 2 ) с образованием
исключительно
a
-галогенпроизводных.

Реакция катализируется кислотами или
основаниями. Скорость реакции не зависит от концентрации и природы галогена.
Процесс протекает через образование енольной формы (медленная стадия), которая
затем реагирует с галогеном (быстрая стадия). Таким образом, галоген не
участвует в скорость
—определяющей стадии
процесса.

Если карбонильное соединение содержит несколько
a
-водородных
атомов, то замещение каждого последующего происходит быстрее, чем предыдущего,
вследствие увеличения их кислотности под действием электроноакцепторного влияния
галогена. В щелочной среде ацетальдегид и метилкетоны дают
тригалогенпроизводные, которые затем расщеплятся под действием избытка щелочи с
образованием тригалогенметанов (галоформная реакция)
.
Расщепление трииодацетона протекает как реакция
нуклеофильного замещения. группы CI
3 — гидроксид-анионом, подобно S
N -реакциям в карбоксильной группе (см. лек. №12).
Иодоформ выпадает из реакционной смеси в виде
бледно-желтого кристаллического осадка с характерным запахом. Иодоформную
реакцию используют в аналитических целях для обнаружения соединений типа
СH
3 -CO-R, в том числе в
клинических лабораториях для диагностики сахарного диабета.
Реакции конденсации.
В присутствии каталитических количеств кислот
или щелочей карбонильные соединения, содержащие
a
-водородные атомы,
претерпевают конденсацию с образованием
b
-гидроксикарбонильных соединений.

В образовании связи С-С участвуют карбонильный
атом углерода одной молекулы (карбонильной компоненты
) и
a
-углеродный атом другой
молекулы (метиленовой компоненты
). Эта реакция носит название альдольной конденсации
(по названию продукта конденсации ацетальдегида –
альдоля).
При нагревании реакционной смеси продукт легко
дегидратируется с образованием
a
,b
-непредельного карбонильного
соединения.

Такой тип конденсации носит название кротоновой
(по названию продукта конденсации ацетальдегида – кротонового
альдегида).
Рассмотрим механизм альдольной конденсации в
щелочной среде. На первой стадии гидроксид-анион отрывает протон из
a
-положения карбонильного
соединения с образованием енолят-аниона. Затем енолят анион как нуклеофил
атакует карбонильный атом углерода другой молекулы карбонильного соединения.
Образующийся тетраэдрический интермедиат (алкоксид-анион) является сильным
основанием и отрывает далее протон от молекулы воды.

При альдольной конденсации двух различных
карбонильных соединений (перекрестная альдольная конденсация) возможно
образование 4-х разных продуктов. Однако этого можно избежать, если одно из
карбонильных соединений не содержит
a
-водородных атомов (например, ароматические альдегиды
или формальдегид) и не может выступать в качестве метиленовой компоненты.

В качестве метиленовой компоненты в реакциях
конденсации могут выступать не только карбонильные соединения, но и другие
С-Н-кислоты. Реакции конденсации имеют препаративное значение, так как позволяют
наращивать цепь углеродных атомов. По типу альдольной конденсации и
ретроальдольного распада (обратный процесс) протекают многие биохимические
процессы: гликолиз, синтез лимонной кислоты в цикле Кребса, синтез нейраминовой
кислоты.
2.3. Реакции окисления и
восстановления
Восстановление
Карбонильные соединения восстанавливаются до
спиртов в результате каталитического гидрирования или под действием
восстановителей, которые являются донорами гидрид-анионов.

[H]: H 2 /кат., кат. – Ni, Pt,
Pd;
LiAlH 4 ; NaBH 4 .
Восстановление карбонильных соединений
комплексными гидридами металлов включает нуклеофильную атаку карбонильной группы
гидрид-анионом. При последующем гидролизе образуется спирт.
Аналогично происходит восстановление
карбонильной группы in vivo под действием кофермента НАД
Н, который является
донором гидрид-иона (см. лек. №19).
Окисление
Альдегиды окисляются очень легко практически
любыми окислителями, даже такими слабыми, как кислород воздуха и соединения
серебра (I) и меди
(II).
Две последние реакции используются как
качественные на альдегидную группу.
В присутствии щелочей альдегиды, не содержащие
a
-водородных атомов
диспропорционируют с образованием спирта и кислоты (реакция Канницаро).
2HCHO + NaOH ® HCOONa + CH 3 OH
Это является причиной того, что водный раствор
формальдегида (формалин) при длительном хранении приобретает кислую
реакцию.
Кетоны устойчивы к действию окислителей в
нейтральной среде. В кислой и щелочной средах под действием сильных
окислителей
(KMnO 4 ) они
окисляются с разрывом связи С-С. Расщепление углеродного скелета происходит по
двойной углерод-углеродной связи енольных форм карбонильного соединения, подобно
окислению двойных связей в алкенах. При этом образуется смесь продуктов,
содержащая карбоновые кислоты или карбоновые кислоты и кетоны.